 其它肿瘤
其它肿瘤
 2020-12-03
2020-12-03
近日,FDA授予双特异性抗体Zanidatamab“突破性疗法”称号,用于治疗先前接受过治疗的HER2基因扩增的胆道癌(BTC)患者。
▌癌症“王中王”胆道癌:几乎无药可用
好医友介绍,胆道癌是指发生在胆道的癌症,包括胆囊癌和胆管癌,约占所有成人癌症的3%。每年全球有超21万人确诊胆道癌,而中国是世界上胆管癌发病率最高的国家之一。
胆道癌早期症状不明显,大多数患者确诊晚期胆道癌后,已失去了手术的机会,加上对肿瘤放化疗均不敏感,基本无药可用。而那些接受根治性手术的患者,其复发率也很高。
对于一线化疗后出现疾病进展的晚期胆道癌患者,目前的标准治疗是以吉西他滨为基础的联合化疗方案,治疗选择十分有限,且疗效并不理想,患者的生存期还不到1年,凶险程度堪比“癌王”胰腺癌。
约5%~19%的胆道癌患者肿瘤过度表达HER2,这类肿瘤细胞生长速度更快,并很快扩散到身体的其他部位。
而目前,尚无HER2靶向疗法获批用于治疗胆道癌,亟待更有疗效的靶向药物。
▌双特异性抗体:Zanidatamab
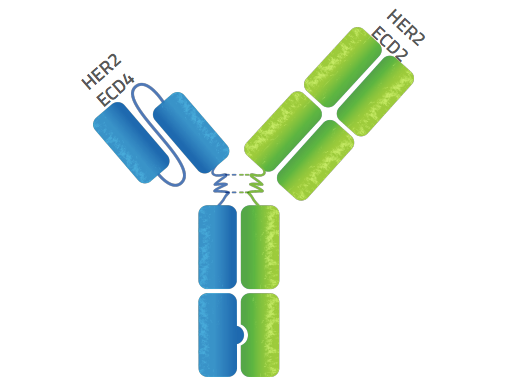
Zanidatamab是一种双特异性抗体,可以同时结合HER2的两个非重叠表位。
这种独特的结合可以产生多种作用机制,包括双重HER2信号阻断、增加HER2蛋白从细胞表面的去除,以及提高细胞毒性作用,从而促进在患者中产生抗肿瘤活性。
目前,该药的临床试验正在全球多地进行,作为表达HER2的实体瘤患者的靶向治疗选择。
先前,FDA还授予Zanidatamab 2个快速通道称号,一种指定用于难治性BTC患者的单一药物,第二种指定用于胃食管腺癌(GEA)患者的一线联合标准化疗。
而根据中国国家药监局药品审评中心(CDE)的最新公示,Zanidatamab已于上个月获得一项临床试验默示许可,针对的适应症为“单药治疗既往接受系统化疗失败的HER2阳性的局部晚期不可切除或转移性胆道癌”。
▌临床数据亮眼,客观缓解率高达66.7%!
好医友得知,这一认定是基于一项正在进行的zanidatamab的1期研究(NCT02892123),该研究在局部晚期、不可切除和/或转移性HER2高表达的(包括BTC)肿瘤患者中进行,主要评估Zanidatamab单药的最大耐受剂量,以及与其他化疗方案联用时的疗效、安全性和耐受性。
具体的试验结果将在1月举行的2021年胃肠道癌专题讨论会(ASCO GI)上发表。而已公布的最新临床试验数据显示:
Zanidatamab作为单药疗法,在治疗HER2基因扩增的经治胆道癌患者时,客观缓解率高达66.7%,疾病控制率达到78.8%。直肠癌和胃癌中的客观响应率分别为46%和39%。
此外,在其他类型的肿瘤中,zanidatamab使胰腺癌患者的靶病变减少100%。中位无进展生存期为5.5个月,且仍在持续评估中。
今年早些时候,Zanidatamab的国际2b期注册研究(NCT04466891)已经启动,入组了约100例年龄≥18对的、经治HER2基因扩增的胆道癌患者。试验的主要终点是客观缓解率,次要终点包括反应持续时间和安全性。
这项新疗法有望成为胆道癌一线治疗方案,改变当前胆道癌缺乏有效治疗手段的临床困境。
▌胆道癌“中国方案”
今年7月,天津医科大学南开临床学院与中国医学科学院基础医学研究所联合团队发表了一篇文章,展示了中国科学家首创的载药囊泡治疗肿瘤技术针对胆管癌治疗的一项临床应用成果:
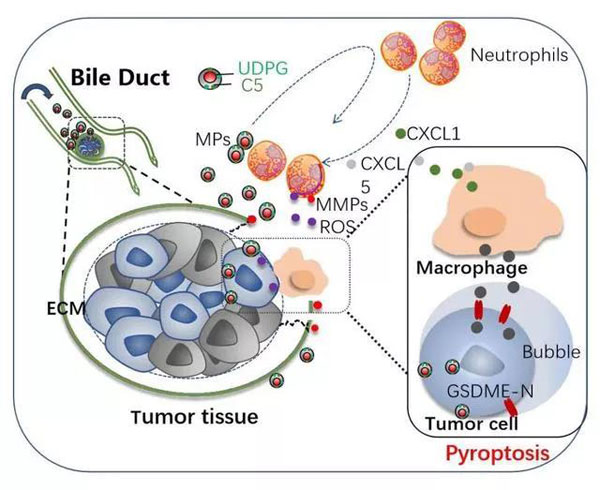
参与临床试验患者中,约30%的患者影像学显示胆道梗阻部分缓解,约有50%患者首次疗程治疗后黄疸症状减轻、肝功能有所恢复,排便颜色由陶土色转为正常的黄色,随访患者中生存期最长达到21个月。
载药囊泡治疗肿瘤技术是一项基于细胞外囊泡来源的、具有天然特性的创新性肿瘤治疗技术,它将来源于肿瘤细胞的囊泡,与微量的化疗药物结合后,将化疗药物富集于囊泡内,并激活免疫反应,用于恶性肿瘤的治疗。
目前,载药囊泡治疗胆管癌技术已在全国多个城市获批使用,用于不能手术的胆管癌患者的治疗。
这项全球首创的新技术,让全球胆管癌胆道腔内治疗实现了从“0”到“1”的突破,未来有望成为胆管癌一线治疗方案。