 神经系统疾病
神经系统疾病
 2021-04-13
2021-04-13
帕金森病是一种常见的神经功能障碍疾病,主要影响中老年人,多在65岁以后发病,是仅次于肿瘤、心脑血管病之后中老年人的“第三大杀手”。
目前,全球约1000多万人患有帕金森病。在我国,就有超300万名患者,且该病已呈现出年轻化趋势。
▌“不死的癌症”——帕金森
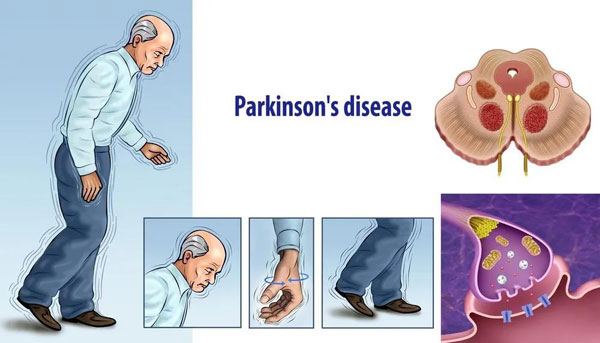
帕金森病的主要症状表现是静止性震颤、运动迟缓、肌肉僵直以及姿势步态异常等运动症状,此外还有注意力减退、痴呆、抑郁、自主神经功能障碍等非运动症状。
帕金森病起病隐匿,病程进展缓慢,多数患者的病程在10年以上,需要终生治疗,也被称为“不死的癌症”。
目前,由于该病呈缓慢加重趋势,且无彻底治愈的办法。因此,治疗目标主要以控制症状,改善患者生活质量为主。临床上常用的有复方左旋多巴、多巴胺受体激动剂、单胺氧化酶抑制剂和抗胆碱药物等。
帕金森病主要是由于大脑黑质发生病变,无法正常分泌多巴胺而导致的。
而导致这一病理改变的确切病因目前仍不清楚,遗传、环境因素、年龄老化等均可能与多巴胺能神经元的变性死亡有关。
此外,除多巴胺系统功能下降外,帕金森病的致病因素还包括α-突触核蛋白聚集、线粒体功能失常、氧化应激等。
▌新通路、新思路!帕金森有望治疗
近日,发表在今年4月《科学进展》杂志上的一篇研究发现:一种激活AMPK的糖尿病药物,不仅可以抑制癌症,也可能有助于恢复神经退行性疾病患者的功能。
“维稳”的线粒体自噬
线粒体自噬是指细胞通过自噬的机制选择性地清除受损线粒体的过程。通常情况下,帕金蛋白会清除被细胞应激破坏的线粒体,使新的线粒体取代它们。这对维持细胞内环境的稳定具有至关重要的作用。
线粒体自噬的调控机制有多种,包括自噬相关基因(ATGs)、PINK1-Parkin途径等等。其中,PINK1/Parkin途径是最主要的途径,且在帕金森等多种疾病的发病中有重要作用。
线粒体自噬的失调将导致多种疾病的发生,如神经退行性疾病(含帕金森)、2型糖尿病、癌症和心血管疾病等。
十多年前,研究人员发现一种名为AMPK的酶,对线粒体损伤等在内的多种细胞应激高度敏感,该酶通过激活一种称为ULK1的酶来控制自噬。随后,研究人员开始寻找由ULK1直接激活的自噬相关蛋白。
研究人员筛选了50多种不同的蛋白之后发现,像线粒体自噬这样重要的过程主要是由三个参与者共同发起——首先是AMPK,然后是ULK1,其次是帕金蛋白。
AMPK可以通过ULK1发出一个“提示”信号输出到帕金蛋白,检查传入的第一波受损线粒体。如有必要,促使不太严重受损的线粒体恢复功能。但在帕金森病患者体内,帕金蛋白发生突变,导致该蛋白无法清除受损的线粒体。
AMPK是细胞新陈代谢的中心传感器,它被一种叫做LKB1的肿瘤抑制蛋白激活,该蛋白与多种癌症有关。
一些药物,如治疗2型糖尿病的二甲双胍可以激活AMPK。同时,大量研究表明,服用二甲双胍的糖尿病患者罹患癌症和衰老合并症的风险较低。因此,二甲双胍目前正在进行“抗衰老”的临床试验。
线粒体自噬是维持细胞内环境稳态的重要一环,但其中的机制比较复杂,相互联系和制衡。
而通过激活AMPK通路,可能有助于恢复神经退行性疾病患者的功能。这也为帕金森病患者的治疗带来了新思路和新疗法。
▌基因疗法值得期待

帕金森病基因疗法领域,也有了新的进展。
去年,在2020国际帕金森病与运动障碍大会(MDS)虚拟会议上,一种腺病毒2型(AAV2)血清载体基因疗法NBIb-1817(VY-AADC)的临床试验数据引起广泛关注。该疗法可编码人类AADC基因,帮助在大脑产生AADC酶,从而将左旋多巴转化为多巴胺。
长达3年的试验研究表明:
NBIb-1817能持续改善患者的运动功能,包括:延长运动功能“开启”期和缩短运动障碍的“关闭”期,降低患者口服药物的需求,而且还显示出疾病分期的改善。
好医友获悉,进一步评估NBIb-1817治疗帕金森病患者安全性和有效性的临床试验正在进行中,值得期待。
数十年来,晚期帕金森病的治疗标准一直没有明显进展,越来越多在研新疗法,有望为帕金森病患者带来新的希望,改善患者生活质量。